Science/Research 詳細
自己整合顕微鏡、超解像度顕微鏡の限界を打破
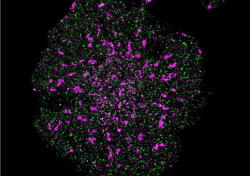
May, 29, 2020, Sydney--ノーベル賞受賞の超解像度顕微鏡の限界を超える超高精細顕微鏡により研究者は、個々の分子間距離を直接計測することができる。
ニューサウスウェールズ大学(UNSW)医療研究者は、無傷細胞内の個々の分子間の相互作用を検出するために単分子顕微鏡で前例のない解像能力を達成した。
2014年ノーベル化学賞は、超解像度蛍光顕微鏡技術が獲得した。これにより顕微鏡の利用者は、細胞内部を初めて見ることができるようになった。これは、複雑な生体系やプロセスに新たな分子的観点を提供するものである。
単一分子顕微鏡の限界が今回、再び破られた。詳細は、Science Advancesに発表されている。
個々の分子は超解像度顕微鏡ですでに観察、追跡できるが、これら分子間の相互作用は、既存の単一分子顕微鏡で改造できる分解能よりも少なくとも4倍小さなスケールで起こる。
「単一分子顕微鏡の局所精度が通常20~30nmである理由は、われわれがその信号を検出している間にその顕微鏡が実際に動くからである。これは不確定性になる。既存の超解像度機器では、われわれはあるタンパク質が他のタンパク質に結合しているかどうかを言うことはできない。それらの距離が、その位置の不確定性よりも短いからである」とUNSW Medicine EMBL Australia Node in Single Molecule Science.、研究チームリーダー、Scientia Professor Katharina Gausは話している。
この問題を回避するためにチームは、単一分子顕微鏡内に、光パスとステージを検出し、再配置する自律フィードバックループを構築した。
「この顕微鏡には、何をするかは問題ではない。基本的にその顕微鏡は、ナノメートル精度でその帰路を見つける。スマート顕微鏡である。それは、オペレータ、サービスエンジニアがする必要がある全てのことをする。また、1秒に12倍の仕事をする」とGaus教授は説明している。
タンパク質間の距離を計測
論文に説明されている設計と方法により、UNSWチームが設計したフィードバックシステムは、既存の顕微鏡に適合しており、サンプル準備で最大の柔軟性が得られる。
「それは、大きなイメージング問題に対する簡素でエレガントなソリューションである。われわれは、顕微鏡の中に顕微鏡を構築しただけである。それがする全ては、主顕微鏡を調整することである。われわれが発見したソリューションは、簡素で実用的であることか本当の強みである。そのシステムのクローニング(複製)は簡単にでき、新しい技術の迅速な取込みも可能だからである」とGaus教授はコメントしている。
超高精度フォードバック単一分子顕微鏡の有用性を実証するために研究チームは、それを使ってT細胞のシグナル伝達タンパク質間の距離の直接計測を実行した。細胞免疫学で有力な仮説は、T細胞受容体が、ブレーキとして働く別の分子の隣にあるときには、これら免疫細胞が静止状態にとどまっていることである。
その高精度顕微鏡は、これら2つのシグナル伝達分子が実際に、活性T細胞内で相互に分離されていることを示すことができた。ブレーキをリリースし、T細胞受容体シグナル伝達をスイッチングする。
「従来の顕微鏡技術は、そのように小さな変化を正確に計測することはできない、静止T細胞、また活性T細胞のこれらシグナル伝達分子間の距離がわすがか4~7 nmしか違わないからである」と同教授は説明している。
「このことは、これらのシグナル伝達機構が、空間的分離の影響をいかに受けやすいかも示している。このように既定のプロセスを特定するためには、精密な距離測定が必要である。また、それはこの顕微鏡が可能にしていることである。これらの成果は、どんな他の手段でも可能でなかった発見に対してこの技術の潜在力を示している」とGaus教授は話している。












 レーザ・光関連製品Webガイド レーザ、オプトエレクトロニクスの最新製品をご紹介します。
レーザ・光関連製品Webガイド レーザ、オプトエレクトロニクスの最新製品をご紹介します。





