Science/Research 詳細
新しいソフトウエアで低解像度cryo-EMマップが焦点を合わせる
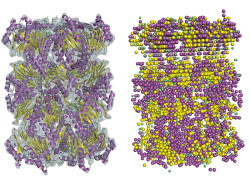
August, 21, 2019, West Lafayette--極低温電子顕微鏡(Cryo-EM)は、タンパク質の構造判定で最もポピュラーな方法である。様々な種類の病気のために研究者の薬剤開発に役立っている。過去数10年で、Cryo-EMはX線結晶学を置き換えた。簡単に大きな結晶に形成できないタンパク質を撮像できるからである。その新技術は、開発者が2017年ノーベル化学賞を獲得できたほどに画期的であった。
Cryo-EMの最終産物は、生物分子における原子密度マップであるが、研究者が必要としているレベルの細部達成には、さらなる解析が必要になる。Nature Methods誌の新研究は、低解像度マップを標準レベルに高める技術を説明している。
研究チームがこれを達成するために用いるアプローチは、出発する詳細度に依存する。2Åおよび3Åのマップは、一般に高解像度と考えられている。しかし、この品質のマップは達成が難しい。また、多くはまだ一般的に4~10Åの範囲で生成されている。2016-18年にElectron Microscopy Data Bankに置かれたすべてのたんぱく質の中で、50%以上は中間分解能であった。
「3よりも高い分解能なら、通常のツールはアミノ酸の位置を探し出し、原子位置のマップを作れる。しかし、cryo-EMは3Åマップはできない」とDaisuke Kiharaは言う。同氏はパデュー大学、生物科学・コンピュータサイエンス教授。「5Å以下のマップでは、通常は、鎖連結は全く見ることができない」。
タンパク質は、実際に、アミノ酸の鎖であり、アミノ基とカルボキシル基とのボンディングが、一定の折り畳みパタンを作る。これらのパタンは、αヘリックスやβストランドとして知られており、タンパク質の二次構造を形成する。
5~8Åのマップでは通常、タンパク質の二次構造の断片は見えるが、チェーン全体は、極めて困難。Emap2secとして知られるKiharaの新方法は、6~10Åのマップで二次構造を明らかにする。
Emap2secは、そのアルゴリズムの中心にディープ畳み込みニューラルネットワーク(CNN)を持つ。これらのネットワークは主に、ディープラーニングシステムで、画像分類、同一性によるそれらの一団化、対象認識に使用される。3Dマップにおけるタンパク質構造同定で機能する。その方法は、情報がニューラルネットワーク層を通過する際に、局所マップ密度の特性をより大きな領域の画像に「畳み込む」からである。局所予測は、マップの大きな領域との関連でなされる。
3Dマップで同定された二次構造は、研究者が、すでにマップに溶け込んでいる既知のたんぱく質構造を割り当てる際に役立つ。つまり、二次構造は出発点、少なくとも構造の一部がどう見えるかの糸口を持つことがある。Emap2secは、研究者が、迅速かつ容易に断片をパズルにはめ込む際に役立つ。同定された構造情報は、構造モデリングに誤りを見つけるさいにも役立つ。
そのプログラムは、ソフトウエア開発プラットフォーム、GitHubで利用できる。
(詳細は、https://news.uns.purdue.edu)












 レーザ・光関連製品Webガイド レーザ、オプトエレクトロニクスの最新製品をご紹介します。
レーザ・光関連製品Webガイド レーザ、オプトエレクトロニクスの最新製品をご紹介します。





