Science/Research 詳細
酸性でも光刺激でオン・オフできる緑色蛍光たんぱく質rsGamillus
August, 22, 2019, 大阪--大阪大学 産業科学研究所の永井健治教授らの研究グループは、pH4.5~9.0の細胞環境で安定して蛍光する、耐酸性の光スイッチ型緑色蛍光たんぱく質“rsGamillus”の開発に成功した。特殊な顕微鏡法と組み合わせることで、光の回折限界を超えた分解能で、生きた生物試料の高解像度画像を撮影できるようになる。
研究グループは昨年、日本産ハナガサクラゲの光る触手から新規の蛍光たんぱく質を単離改変することによりpH4.5~9.0の細胞環境で安定して蛍光する耐酸性の緑色蛍光たんぱく質“rsGamillus”を開発した。
今回、吸収スペクトル測定とX線結晶解析により、酸性環境下において、Gamillusの蛍光・非蛍光状態が光刺激により可逆的に切り替わること(光スイッチ)、そのメカニズムが蛍光発色団のtrans-cis異性化並びにフェノール水酸基のプロトン化/脱プロトン化であることを見いだした。このメカニズムを基にした分子設計、遺伝子変異導入により、光スイッチのコントラストを向上させた変異体rsGamillusを開発した。
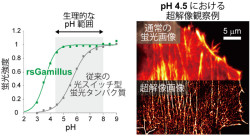
現在までに報告されている可逆的光スイッチ蛍光たんぱく質が全てpH5~6以下の酸性環境で蛍光を失うのに対して、rsGamillusは酸性環境でも安定した蛍光を放ち、細胞内のほぼ全てのpH環境で使用可能であることが分かった。人工的に模した細胞酸性環境中(pH4.5)で、1分子蛍光の輝点重心位置の計測に基づく超解像顕微鏡観察に応用できることを証明した。酸性細胞小器官は、2016年のノーベル医学・生理学賞受賞者の大隅良典博士が発見したオートファジーなど、多くの生命機能に密接に関わっている。しかし、既存の光スイッチ型の蛍光たんぱく質は、低pHで蛍光しないため、酸性細胞小器官内での使用が限られていた。
rsGamillusは、酸性環境中の未知の生命現象を発見するための基盤技術となり、医学・創薬研究にも大きく貢献すると期待される。
研究成果は、2019年8月15日に「Cell Chemical Biology」(オンライン)に掲載された。
(詳細は、https://www.jst.go.jp/)


















