Science/Research 詳細
アダブティブオプティクス3D顕微鏡、超解像度細胞イメージング
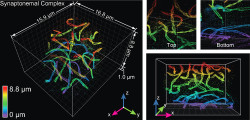
August, 18, 2016, West Lafayette--複数の大学の共同研究チームによると、新しい超高解像度「ナノスコープ」は、細胞全体とその細胞構成要素を前例のない詳細さで3D画像に撮ることができる。これは、これまでに見られなかった生物学的現象を明らかにし、新たな医療洞察をもたらす進歩である。
この技術は、蛍光顕微鏡と超解像度顕微鏡のいくつかのイノベーションを含んでおり、天文学で使用される「適応型オプティクス」(adaptive optics)、光歪を補正するために形を変える可変ミラー(deformable mirror)と同種の技術を利用している。天文学では、可変ミラーは天体の鮮明画像を作りだすために大気の歪みを補正する用途で使用される。可変ミラーは、光が生物組織を透過する際に起こる歪を打ち消すためにも使用できる。
超解像度蛍光顕微鏡は、2014年、科学でノーベル賞を受賞し、生物学研究では重要なツールになっている。しかし、サンプル表面の奥深いところの特徴の解像に課題があるために、その利用には限界がある。
研究チームは、新システム、全細胞4Pi単一分子切替ナノスコピー(W-4PiSMSN)の開発によってそうした問題を解決した、とパデュー大学(Purdue University)生体医用工学准教授、Fang Huangは説明している。
新システムは、可変ミラーを顕微鏡に組み込むことによって元の超解像度蛍光顕微鏡を改良している。利用したのは2つの対物レンズで、1つはサンプルの上、もう1つはサンプルの下に入れ、細胞内部深くにあるタンパク質の分子位置を正確に狙う一連の新しいアルゴリズムを導入している。
このシステムにより研究者は、光波長よりもはるかに小さな詳細部分を解像することができ、強力で用途の広い新しいラボツールが実現している。
「光の波の性質が従来の光学顕微鏡の解像度を200nm程度に制限しており、細胞以下の構造やタンパク質集合の詳細は解像できない」とHuangは言う。
しかし新しいシステムは、哺乳類細胞全体で、細胞成分を3Dで、10~20nmの解像度でイメージングできるので、ウイルスの微細な特徴を再構成できる強力なツールとなる。これまで、そのような細部は、電子顕微鏡でしか見ることができなかった。しかし、電子顕微鏡では、サンプルの取り扱いで細胞を殺す必要がある。
「目標の1つは、最近の超解像度技術の2つの主要障害である、生きた細胞と組織のイメージングの方向に限界を広げることである。したがって、生理学的な条件で生きている細胞機能をナノスケールで可視化することである」とHuangは語っている。
細胞内の分子や細胞小器官の構造は、「光でスイッチできる」蛍光タンパク質、有機染料でタグ付けすることができる。これらは、少量のUV光に晒されると光る。
「これらの特別な蛍光タグ(蛍光色素分子)には、ONとOFFの2つの状態がある。これらの分子に光を照射することで、ON/OFF状態をコントロールすることができる。単一分子スイッチングナノスコピーの概念は、多様な時間フレームで分子を確率的にON、OFFし、単一分子の正確な位置をピンポイントで示し、超解像度で細胞成分を再構築することである」。
超解像度イメージングは、数千から数100万の単一分子の位置から再構築される。


















