Science/Research 詳細
ガン増殖を抑える仕組み、がんの強力な”ブレーキ役”分子、DA-Rafのメカニズム
January, 7, 2026, 千葉--千葉大学大学院理学研究院の高野和儀助教らの研究グループは、神戸大学バイオシグナル総合研究センターの伊藤俊樹教授、辻田和也准教授と共同で、がんの増殖に深く関わる「Ras-ERK経路」を抑える分子「DA-Raf」が、細胞膜の脂質に結びつくことで、がんの原因となるシグナルを効率よく遮断する仕組みを世界で初めて明らかにした。
この発見は、がん治療薬の新しい開発ターゲットとなるだけでなく、細胞膜で起こる様々な生命現象を操作する技術革新にもつながる可能性がある。
研究の成果
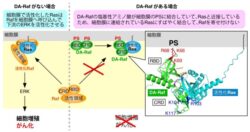
研究グループは、DA-Rafがどのようにして強力な“ブレーキ役”として働くのかを調べた。その結果、DA-Rafは細胞膜に含まれる脂質(ホスファチジルセリン(PS)に結合することで、あらかじめ細胞膜に局在し、Rasに優先的に結びつくことがわかった。これにより、がんの原因となるRas-ERK経路の働きを効果的に抑えていることを初めて解明した。
まず、細胞内での膜-タンパク質結合を詳しく解析したところ、DA-Rafの「Ras結合領域(RBD)」と「システインに富む領域(CRD)」の両方にある塩基性アミノ酸が協力して細胞膜と結合することがわかった。これによってDA-Rafは細胞膜上でRasの近くに配置され、結果的にRasとの結合力が高まった。例えるなら、磁石を近づけたときに吸い寄せられるように、結合の効率が増す仕組み。
さらに、細胞膜に結合できないように改変したDA-Raf(DA-Raf(RBD変異体))では、Ras-ERK経路の抑制効果が失われることも確認された。逆に、細胞膜への結合を人工的に取り戻させると、再び強い抑制作用を示した。つまり、DA-Rafが細胞膜に結合することが、がん抑制機能の“決め手”であることが証明されたのである。これを椅子取りゲームに例えるなら、DA-Rafは予めRasの近くの椅子を占領することで、Rafが座る余地をなくしている。
今回の研究で示されたDA-Rafの独自の働きは、Ras-ERK経路の異常が関与する、がんや筋萎縮症などの疾患の治療に向けた新しいアプローチとなる可能性がある。研究チームは今後、DA-Rafの細胞膜での動きや、他のRas関連因子との関係性をさらに詳しく調べることで、創薬への応用を目指す。
研究成果は、10月21日に国際学術誌Life Science Allianceに掲載された。
(詳細は、https://www.kobe-u.ac.jp)


















