Science/Research 詳細
貼れる無線給電式発光デバイスを用いた光がん治療システム
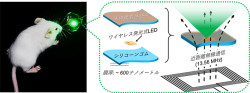
July, 24, 2018, 東京--早稲田大学 高等研究所の藤枝俊宣准教授、先進理工学研究科の山岸健人博士、理工学術院の武岡真司教授は、防衛医科大学校 生理学講座の守本祐司教授らの研究グループと共同で、生体組織表面にシールのように貼り付けられる体内埋め込み型の発光デバイスを開発した。このデバイスを担がんモデルマウスの体内に移植することで光がん治療に応用し、腫瘍を消失させることに成功した。
体内埋め込み型の発光デバイスの研究や開発は近年、盛んに行われており、厚さミリメートルの薄膜状デバイスが数多く報告されている。小型化した発光デバイスを体内の腫瘍直下に貼り付けて固定し、無線給電式に点灯できれば、従来法では困難だった体内深部の臓器にできたガンを治療できる新たな医療技術として大いに期待されている。しかし、腫瘍と光源の位置が少しでもずれると腫瘍に蓄積した光増感剤を効率よく励起できず、治療効果が得られないため、生体内の臓器や組織上で長期間安定に固定できる体内埋め込み型の発光デバイスの開発が望まれていた。
研究グループは、柔軟性や伸縮性に優れるシリコーン製の高分子ナノ薄膜(膜厚約600nm)の表面に生体模倣型接着分子であるポリドーパミン(Polydopamine: PDA)をコーティングすることで、厚さミリメートルのシリコーン薄膜に対して生体組織への接着性を25倍向上させ、小型デバイスを縫合なしで生体内に2週間以上、安定に固定することに成功した。また、無線給電式のLEDチップ(赤・緑)を担がんモデルマウス体内の腫瘍直下に固定し、無線給電アンテナを用いて10日間連続的に点灯させ、腫瘍を消失させることにも成功した。
研究では、光源を腫瘍の間近に設置できるので、従来型の光ガン治療で用いられているレーザ光の1000分の1の光の強さのLEDでも顕著な腫瘍消失効果が得られた。さらに、これまで組織透過性の観点から「生体の窓」と呼ばれる近赤外光しか使われてこなかった光ガン治療において、デバイスを体内埋め込み型にすることで、緑色光を用いた治療効率の高い光ガン治療を世界に先駆けて実現した。
無線給電式・埋め込み型光がん治療の臨床応用が実現すれば、負担が少ない次世代型がん治療法として、将来、患者に恩恵をもたらすと期待される。
研究成果は、Nature Biomedical Engineeringオンライン速報版で公開された。
(詳細は、www.jst.go.jp)




















