Science/Research 詳細
生きた標本から複雑な光散乱情報を捉える
August, 22, 2023, Boston--ボストン大学の研究者は、複数のタイプの光散乱を示す生体サンプルの3D屈折率分布を回復する新しいアルゴリズムを開発した。そのアルゴリズムは、強度回折トモグラフィ(IDT)という新しいイメージングアプローチの最適化に役立つ。
ボストン大学のJiabei Zhuは、Optica Imaging Congressでこの研究について発表した。
「3D定量位相イメージング(QPI)は、バイオメディカルイメージング分野の様々なアプリケーションに優れた機能がある。ラベルフリー技術としてQPIは、サンプルを損傷する光毒性効果を誘発する外因性造影剤や染料なしで透明な生き物や細胞をイメージングできる。従来の位相差や微分干渉コントラスト顕微鏡と比べてQPIは、高コントラスト形態学的情報だけでなく、定量的位相情報も提供する。特に3D QPIは、サンプル内の高分解能3D屈折率分布を提供できる。この貴重な情報は、血液学、神経学、免疫学の研究を促進し、病気や感染の診断に役立つ」(Zhu)。
3Dイメージング技術を使って厚い生体サンプルを調べることができるが、高速取得と高分解能の両方を達成することは、簡単ではない。IDTアプローチは、この限界を克服するラベルフリー位相トモグラフィ技術である。同技術は、標準的な顕微鏡に簡単に追加できるプログラマブルLEDアレイを使って実行できる。
研究チームは、先頃、環状IDT(aIDT)および多重IDT(mIDT)として知られる2つのIDT法を開発した。これらは、動的生体サンプルを可視化できるように画像取得スピードを増強する。環状IDT(aIDT)は、対物レンズの開口数に一致するLEDリングを使用する。また、多重IDT(mIDT)は、複数のLEDsを使ってサンプルを同時照射する。
既存のIDT再構成アルゴリズムが、高NA対物レンズの利用により、新しいアプローチでうまく機能しないことが分かったのでチームは、新しいアルゴリズムを開発することにした。それは、スプリットステップ非近軸(SSNP)法ベースのマルチ散乱モデルを使う。これは、光回折トモグラフィの類似制約を克服するために最近開発された。
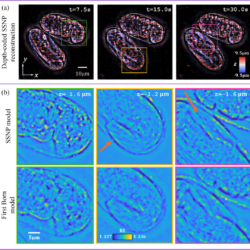
研究チームは、aIDTを使って新しいIDT再構成アルゴリズムを頬上皮細胞に適用すると、様々な深さで細胞の識別が容易にできることを示した。また、細胞境界や膜の再構成、細胞周りの在来細菌の可視化も容易にできることを示した。チームは、mIDTを使い、それを厚いマルチ散乱生Cエレガンス(C. elegans)胚にも適用した。結果としての再構成画像は、線虫の折り畳み方の詳細を示しており、単一深さ横断面は、その細胞の輪郭の形態学的詳細、頬腔、線虫のテールを示していた。
全般的に実験は、SSNP法をIDTに拡大することで、広視野で高品質画像を達成できることを示した。














