Science/Research 詳細
新しい顕微鏡法でアミロイドたんぱく質構造を見る
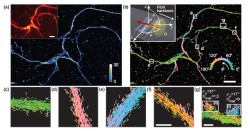
August, 21, 2020, Washington--アルツハイマやパーキンソンなどの神経変性病は、脳内に凝集した、異常な折り畳みのアミロイドタンパク質を伴うことがよくある。新開発の技術は単分子の方向を計測するもので、これにより光学顕微鏡を使って、これらの問題のあるタンパク質の構造についてナノスケールの細部を初めて明らかにすることがであるようになる。
ワシントン大学セントルイスの研究チームは、新しいアプローチをOpticaに発表した。
「アルツハイマ病やパーキンソン病などの神経変性疾患は、世界中で死亡の主因となっている。われわれの単一分子配向イメージングアプローチが、アミロイド構造に新たな洞察を提供し、将来、こうした疾患に対する効果的な治療学の開発に貢献できることを願っている」と論文の共同著者、Tianben Dingはコメントしている。
脳の生物学的、化学的プロセスは、分子間の複雑な動きと相互作用によって推進されている。ほとんどのアミロイドタンパク質は非毒性であるが、ほんのわずかなミスフォールディングが、結果的に多くのニューロンを殺すことになる。
「われわれは、病気の基本的な生物学的メカニラズムを理解するために、生きたシステム内のこれらの分子の動きを見ることができるイメージング技術を必要としている。アルツハイマ病やパーキンソン病、糖尿病など、アミロイドとプリオンタイプの病気は、この技術のためのわれわれの最初のターゲットであるが、それは、多くの他の領域にも適用されるとわれわれは見ている」と研究チームリーダー、Matthew D. Lewは説明している。
ベストの顕微鏡を選択
Lewの研究室は、いくつかの単一分子超分解能顕微鏡法を開発した。これは、単一タンパク質に付着した蛍光分子の配向と位置を計測するものである。配向情報は、サンプルの蛍光の位置だけでなく、その光の特性、偏光などを計測することで得られる。これらは、ほとんどの他の顕微鏡アプローチでは一般に無視されている。
Opticaの記事で、研究者は、様々な顕微鏡が蛍光分子の方向をいかに高感度に計測するかを特性評価するために設計した性能測定基準について説明している。その新しい性能指標を利用して研究者は、蛍光の光を2つの偏光チャネル(x and y)に分離する顕微鏡が、優れた、また実用的な方向計測を提供することを確認した。
研究の共著者、Tingting Wuは、「われわれが開発した測定基準は、特殊顕微鏡設計の計算性能を以前よりも1000倍高速にする。アミロイド集団に結び付いた単一分子の方向を計測することで、選択された顕微鏡によりわれわれは、アミロイド構造組織の差をマッピングすることができた。これは、標準的な局所顕微鏡ではできないことである」とコメントしている。
蛍光プローブとアミロイド表面との間に人工的リンクが全くないので、アミロイド表面へのプローブの結合方向は、アミロイドタンパク質自体がどのように組織されるかについて情報を持っている。研究チームは、アミロイドタンパク質に付着するたびに蛍光分子の方向がどのように変わるかを定量化した。この結合動作の差は、アミロイド集団間の構造差に帰着できる。その方法が、単分子情報を提供するので、研究チームは、局所的特徴の細部を平均化することなく、アミロイド構造間のナノスケール差を観察できた。
長期研究の機会
「われわれは、その方法を拡張してアミロイド構造内および構造間のナノスケールの変化をモニタする計画である。アミロイドは何時間、何日もかけて構造化するからである。アミロイド集団の長期研究により、アミロイドタンパク質がどのように組織化され、どの程度速くそれらが成長するか、自然に消滅するか、その新たな相互関係が明らかになる」(Ding)。
研究者は、配向-位置顕微鏡で用いたセットアップは、商用入手可能なパーツで構成されている単一分子超解像度顕微鏡を利用するものならだれで入手できる、と指摘している。その分析コードは、https://github.com/Lew-Lab/RoSE-Oで入手可能。
「光学顕微鏡とイメージングでは、科学者とエンジニアは、イメージングの限界を押し広げ、より高速にしようとしている。また一段と深くプローブし、解像度を高めようとしている。われわれの研究は、分子配向に焦点を合わせることで生物学における基本的プロセスに光を当てることができることを示した。これにより、従来の顕微鏡では可視化できない生物学の内部構造細部が明らかにできる」とLewはコメントしている。














