Science/Research 詳細
ガラスバブル・ナノキャリア、膵臓ガン治療効果増進
October, 28, 2022, Los Angels--過去30年、ガンの早期発見と治療が、死亡率全体を30%以上減らすのに役立った。しかし、膵臓ガンは、処置が難しいままである。診断後5年生存するのは、9人のうち1人だけ。一つには、このガンが、処置に対する抵抗を助ける生物学的要素で守られているからである。
流れを変えることを目指してUCLAの研究チームは、膵臓ガンの併用療法を行う技術を開発した。これは、膵臓ガンの薬物療法の一部として承認された化学療法薬、イリノテカンを搭載したナノスケール粒子と試験研究中の薬3M-052を使う。これにより、免疫活動強化、腫瘍の抵抗を克服できる。
ACS Nanoに発表された研究でチムは、膵臓ガンマウスモデルで、同時提供併用療法が、その部分の合計より優れていることを示した。
責任著者、UCLAカリフォルニアナノシステム研究所リサーチディレクタ、André Nelは、私見として、「免疫系を誘い出すことは、膵臓ガンで非常に優れた処置結果を出す上て大きな差になる。それこそが、この研究でわれわれが到達したいところである」とコメントしている。
研究者の二重ロードナノキャリアは、縮小しつつある腫瘍には、ナノキャリアのないイリノテカン、あるいは2つの薬剤を独立にデリバリーするナノキャリアのいずれと比べても、効果的であり、マウスではガン転移を抑制した。併用療法は、腫瘍部位に、より多くのガンを殺す免疫細胞を引きつけ、血中の薬剤レベルを長く維持した。有害な副作用の証拠はなかった。
ガン細胞の成長を阻止することに加えて、イリノテカンは、免疫系の樹状細胞に危険信号を送る。次にこれらがキラーT細胞を動員する。すると、それらが腫瘍部位に向かい、ガン細胞を破壊する。しかし、樹状細胞は、膵臓ガン患者で機能障害を起こすことかよくある3M-052が、特別に支援し、ガン部位と近傍のリンパノードの両方で、それらが改善されたマーシャルキラーT細胞になるのを助ける。
ガンにとって併用療法は新しくないが、同じナノキャリアに薬剤をいっしょに詰め込むことは難しいと分かっている。化学療法には、一つだけのデュアルデリバリナノキャリアが、FDAによって承認されている。しかし、過去7年で、Nelラボは、同時デリバリのアプローチを開発した。今回の成果は、その革新的ナノキャリア設計が、それらが別々にデリバーされるよりも、より効果的に協力して効力を発揮できるというさらなる証拠を示している。
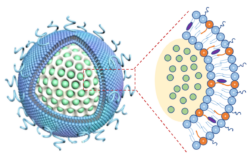
ほとんどのナノキャリアは、細胞膜に類似した脂肪質でできた脂質分子の層で構成されており、薬剤が詰め込めるスペースがある。新しいデバイスで、その脂質二重層が、シリカでできたガラスバブルを取り囲む。その中空内部をイリノテカンで満たすことが可能である。巧妙な新案でUCLAポスドク研究者、筆頭著者、Lijia Luoは、その3M-052分子の脂肪質テールが第2の薬剤を直接これら外脂質層に組み込めると考えた。
キャリアの構造的設計は、人間の髪の毛の幅に1000個位が入るほど小さく、薬剤漏洩を阻止し、デバイスが膵臓ガンを保護しいる手強いロープのような障壁に入り、腫瘍部位に移動する際に毒性の阻止に役立つ。ガラスバブルは、さらなる漏洩を保護し、他の薬剤キャリアと比べて、キャリアが、より多くのイリノテカンを腫瘍部位にデリバーできるようにする。
チームは、大きな動物モデルでその処置をテストするためにさらなる前臨床実験を行い、そのシリカナノキャリアの量産で品質制御を確認する。
(詳細は、https://newsroom.ucla.edu/)


















